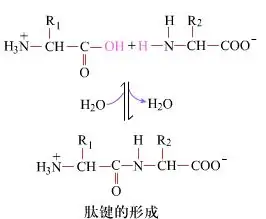
Na powierzchni tworzenie wiązań peptydowych, dipeptydów, jest prostym procesem chemicznym. Oznacza to, że dwa składniki aminokwasowe są połączone wiązaniem peptydowym, wiązaniem amidowym, podczas gdy są odwodnione.
Tworzenie wiązań peptydowych jest aktywacją aminokwasu w łagodnych warunkach reakcji. (A) ugrupowanie karboksylowe, drugi aminokwas (B) Nukleofilowy aktywowany ugrupowanie karboksylowe tworzy następnie dipeptyd (A-B). „Jeśli komponent karboksylowy (A) nie jest chroniony, tworzenie wiązania peptydowego nie można kontrolować”. Produkty uboczne, takie jak peptydy liniowe i cykliczne, można mieszać ze związkami docelowymi A-B. Dlatego wszystkie grupy funkcjonalne niezbędne do tworzenia wiązań peptydowych muszą być chronione w sposób tymczasowo odwracalny podczas syntezy peptydu.
Tak więc synteza peptydów - tworzenie każdego wiązania peptydowego - obejmuje trzy etapy agregacji.
Pierwszym krokiem jest przygotowanie niektórych aminokwasów, które wymagają ochrony, a struktura ztolioniowa aminokwasów już nie istnieje.
Drugim krokiem jest dwustopniowa reakcja na tworzenie wiązań peptydowych, w której grupa karboksylowa aminokwasu chronionego N najpierw jest aktywowana do aktywnego pośredniej, a następnie powstaje wiązanie peptydowe. Ta sprzężona reakcja może wystąpić albo jako reakcja jednoetapowa lub jako dwie sekwencyjne reakcje.
Trzecim krokiem jest selektywne usuwanie lub całkowite usunięcie podstawy ochronnej. Chociaż całe usunięcie może wystąpić dopiero po złożeniu wszystkich łańcuchów peptydów, konieczne jest również selektywne usunięcie grup ochronnych w celu kontynuowania syntezy peptydów.
Ponieważ 10 aminokwasów (Ser, Thr, Tyr, ASP, Glu, Lys, Arg, His, Sec i Cys) zawiera grupy funkcjonalne łańcucha bocznego, które wymagają selektywnej ochrony, dzięki czemu synteza peptydów jest bardziej skomplikowana. Tymczasowe i półtrwałe podstawy ochrony należy odróżnić ze względu na różne wymagania selektywności. Tymczasowe grupy ochrony są używane w następnym etapie, aby odzwierciedlić tymczasową ochronę grup funkcjonalnych aminokwasów lub karboksylowych. Półprzewodowe grupy ochronne są usuwane bez zakłócania już utworzonych wiązań peptydowych lub łańcuchów bocznych aminokwasów, czasem podczas syntezy.
„Idealnie, aktywacja komponentu karboksylowego, a następnie tworzenie wiązań peptydowych (reakcje sprzęgania) powinny być szybkie, bez tworzenia rasowego lub produktu ubocznego, a reagenty molowe należy zastosować w celu osiągnięcia wysokiej wydajności.” Niestety żadna z metod sprzężenia chemicznego nie spełnia tych wymagań, a niewiele jest odpowiednich do praktycznej syntezy.
Podczas syntezy peptydów grupy funkcjonalne zaangażowane w różne reakcje są zwykle powiązane z centrum ręcznym, a glicyna jest jedynym wyjątkiem, a istnieje potencjalne ryzyko obrotu.
Ostatnim krokiem w cyklu syntezy peptydów jest usunięcie wszystkich grup ochronnych. Selektywne usunięcie grup ochronnych jest ważne dla rozszerzenia łańcucha peptydowego oprócz wymogu całkowitego usunięcia ochrony w syntezie dipeptydu. Strategie syntetyczne powinny być starannie zaplanowane. W zależności od strategicznego wyboru N może selektywnie usunąć grupy chroniące α-amino lub karboksyl. Termin „strategia” odnosi się do sekwencji reakcji kondensacji poszczególnych aminokwasów. Zasadniczo istnieje różnica między stopniową syntezą a kondensacją fragmentu. Synteza peptydów (znana również jako „konwencjonalna synteza”) występuje w roztworze. W większości przypadków stopniowe wydłużanie łańcucha peptydowego można syntetyzować jedynie za pomocą łańcucha peptydowego do syntezy krótszych fragmentów. Aby zsyntetyzować dłuższe peptydy, docelowe cząsteczki muszą być podzielone na odpowiednie fragmenty i ustalić, że mogą zminimalizować stopień różnicowania na końcach C. Po stopniowym montowaniu poszczególnych fragmentów związek docelowy zostanie połączony. Strategia syntezy peptydów obejmuje wybór najlepszego i najbardziej odpowiedniego fragmentu ochronnego, a strategia syntezy peptydów obejmuje wybór najbardziej odpowiedniej kombinacji zasad ochronnych i najlepszą metodę koniugacji fragmentu.
Czas postu: 2025-07-02