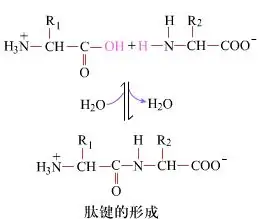
Sur la surfaco, la formado de peptidaj ligoj, produktantaj dipeptidojn, estas simpla kemia procezo.Ĉi tio signifas, ke la du aminoacidkomponentoj estas ligitaj per peptida ligo, amida ligo, dum ili estas senhidratigitaj.
Peptida ligoformado estas la aktivigo de aminoacido sub mildaj reagkondiĉoj.(A) karboksila parto, dua aminoacido (B) La nukleofila aktivigita karboksila parto tiam formas la dipeptidon (AB)."Se la karboksila komponanto (A) ne estas protektita, la formado de la peptida ligo ne povas esti kontrolita."Kromproduktoj kiel ekzemple liniaj kaj ciklaj peptidoj povas esti miksitaj kun celkunmetaĵoj AB.Tial, ĉiuj funkciaj grupoj ne implikitaj en peptidobliga formado devas esti protektitaj en provizore reigebla maniero dum peptidsintezo.
Do, peptida sintezo - la formado de ĉiu peptida ligo - implikas tri paŝojn de agregado.
La unua paŝo estas prepari kelkajn aminoacidojn, kiuj bezonas protekton, kaj la zwitteriona strukturo de aminoacidoj ne plu ekzistas.
La dua paŝo estas du-ŝtupa reago por formi peptidajn ligojn, en kiu la karboksila grupo de la N-protektita aminoacido unue estas aktivigita al la aktiva intera kaj tiam la peptida ligo estas formita.Tiu kunligita reago povas okazi aŭ kiel unupaŝa reago aŭ kiel du sinsekvaj reagoj.
La tria paŝo estas la selektema forigo aŭ kompleta forigo de la protekta bazo.Kvankam ĉiu forigo povas nur okazi post kiam ĉiuj peptidĉenoj estis kunvenitaj, selektema forigo de protektaj grupoj ankaŭ estas postulata por daŭrigi peptidsintezon.
Ĉar 10 aminoacidoj (Ser, Thr, Tyr, Asp, Glu, Lys, Arg, His, Sec kaj Cys) enhavas flankajn ĉenajn funkciajn grupojn, kiuj postulas selekteman protekton, igante peptidan sintezon pli komplika.Provizora kaj duon-permanenta protektobazoj devas esti distingitaj pro la malsamaj postuloj por selektiveco.Portempaj protektogrupoj estas uzataj en la sekva paŝo por reflekti la provizoran protekton de aminoacido aŭ karboksilaj funkciaj grupoj.Semi-permanentaj protektaj grupoj estas forigitaj sen interfero kun jam formitaj peptidaj ligoj aŭ aminoacidaj flankaj ĉenoj, foje dum sintezo.
"Ideale, aktivigo de la karboksila komponento kaj posta formado de peptidaj ligoj (kunligaj reagoj) devus esti rapidaj, sen racema aŭ kromprodukta formado, kaj molaraj reakciantoj devus esti aplikataj por atingi altajn rendimentojn."Bedaŭrinde, neniu el la kemiaj kunligaj metodoj kontentigas tiujn postulojn, kaj malmultaj taŭgas por praktika sintezo.
Dum peptidsintezo, la funkciaj grupoj implikitaj en diversaj reagoj estas kutime ligitaj al la mana centro, glicino estas la nura escepto, kaj ekzistas ebla risko de rotacio.
La fina paŝo en la peptida sinteza ciklo estas la forigo de ĉiuj protektaj grupoj.Selektema forigo de protektaj grupoj estas grava por peptidĉetenendaĵo aldone al la postulo por kompleta forigo de protekto en dipeptidsintezo.Sintezaj strategioj devas esti zorge planitaj.Depende de la strategia elekto, N povas selekteme forigi la α-amino aŭ karboksilaj protektaj grupoj.La esprimo "strategio" rilatas al la sekvenco de kondensaj reagoj de individuaj aminoacidoj.Ĝenerale, estas diferenco inter laŭgrada sintezo kaj fragmenta kondensado.Peptida sintezo (ankaŭ konata kiel "konvencia sintezo") okazas en solvaĵo.Plejofte, laŭpaŝa plilongigo de la peptidĉeno povas nur esti sintezita uzante la peptidĉenon por sintezi pli mallongajn fragmentojn.Por sintezi pli longajn peptidojn, la celmolekuloj devas esti segmentitaj en konvenajn fragmentojn kaj determinitaj ke ili povas minimumigi la gradon da diferencigo ĉe la C-finstacio.Post kiam la individuaj fragmentoj estas iom post iom kunmetitaj, la cela kunmetaĵo estos kunigita.La strategio de peptida sintezo inkluzivas la elekton de la plej bona kaj plej taŭga protekta fragmento, kaj la strategio de peptida sintezo inkluzivas la elekton de la plej taŭga kombinaĵo de protektaj bazoj kaj la plej bona metodo de fragmenta konjugacio.
Afiŝtempo: Jul-19-2023